falseit is false
falseit is false
falseit is false
falseit is false
falseit is false
falseit is false
falseit is false
falseit is false
falseit is false
true
it is true
falseit is false
متن زیر مروری چند خطی بر آزمونی است در باره پیوند کبد که در پایین همین صفحه شروع خواهد شد . بنابر این اگر بر عکس رزیدنت ها حوصله تست زدن !! ندارید به همین مقدار اکتفاء کنید.ضمنا اگر اشتباهی در این درس دیدید ، محبت کنید و تذکر دهید.
مرجع :
بیهوشی میلر ۲۰۱۵ : صفحات ۲۲۷۴ الی ۲۲۸۹ / ۵۳۷ / ۱۸۵۰/ ۲۹۰۸ / ۵۸۰ الی ۵۸۱ / ۲۲۵۸ الی ۲۲۵۹/ ۲۷۸۵ الی ۲۷۸۶/ ۲۲۵۳ الی ۲۲۵۴ / ۲۲۴۷ الی ۲۲۴۹/ ۳۰۳۴/ ۳۰۴۶ الی ۳۰۴۷/ ۳۱۵۳/ ۳۲۲۲/ ۲۲۶۲ الی ۲۲۶۳/ ۲۲۹۷ الی ۲۲۹۹/ ۲۳۰۳ الی ۲۳۰۵/ ۲۰۱۴/ ۲۸۳۹/ ۲۲۹۲/ ۲۶۵۸/ ۲۴۴۶/ ۲۹۴۴/ ۲۲۴۴/ ۲۲۲۸/ ۲۲۸۹/ ۲۴۳۹/ ۱۱۲۲/ ۱۱۳۷/ ۱۱۸۴/ ۱۹۳۱ الی ۱۹۳۲/ ۱۰۶۰/ ۱۲۱۱/ ۱۸۰۸/ ۱۸۴۵/ ۱۸۴۷ الی ۱۸۴۸/ ۱۸۸۷/ ۱۸۸۹/ ۱۸۹۲/ ۵۶۱/ ۵۲۱/ ۵۳۳/ ۵۴۰/ ۸۹۱/ ۸۹۲/ ۸۵۴/ ۹۸۸
کواگزیست ۲۰۱۸ : صفحات ۳۵۰ الی ۳۵۸/ ۳۴۸ / ۷۷ / ۱۰۳ / ۱۰۵/ ۳۵۲/ ۳۷۰/ ۴۴۲/ ۴۹۵/ ۵۱۶/ ۵۲۳/ ۵۳۰/ ۶۰۷/ ۵۰۹/ ۳۰۳ الی ۳۰۵/ ۶۵ الی ۶۶ / ۳۴۵
مراقبت های ویژه فینک ۲۰۱۷ : صفحات ۹۰۴ الی ۹۰۶ /
==================================================================================================================
اولین جراحی که اقدام به پیوند کبد بر روی انسان کرد چه کسی بود ؟
دکتر توماس استارزل (Thomas Starzl) ( میلر ص ۲۲۷۴)
=================================================================================================
امتیاز MELD معرف چه چیزی است ؟
MELD مخفف این عبارت است :
Model for End-Stage Liver Disease
برای محاسبه امتیاز MELD از فرمولی استفاده می کنند که ( حفظ آن کار من و شما نیست !! و ) نیاز به سه متغیر زیر دارد :
الف) بیلی روبین سرم ب) INR ج) کراتینین سرم ( میلر ص ۲۲۵۳)
برای اینکه اجزای MELD score یادمان نرود از لوگوی شرکت بیک سوء استفاده کردیم ( باور کنید یک ریال هم نداده اند!)

امتیاز MELD چه ارتباطی با خطرات حول و حوش عمل بیماران کبدی پیشرفته دارد ؟
هر چه این امتیاز بالاتر باشد خطرات بالاتر می رود چنانکه با امتیاز ۱۵ و بالاتر خطرات حول و حوش عمل ( بیماران غیرپیوندی و الکتیو) افزایش می یابد ( میلر ص ۱۱۲۰ و ۱۱۲۲) . در کواگزیست اینگونه نوشته که بیماران با امتیاز بالای ۱۵ نباید تحت جراحی الکتیو قرار گیرند. ( ص ۶۵)
حداقل امتیاز MELD برای انجام پیوند کبد چند است ؟
برای اینکه مزایای انجام پیوند کبد بیشتر از خطرات آن باشد ، این امتیاز حداقل باید ۱۸ باشد.( کواگزیست ص ۶۵)
— در ارزیابی های انجام شده ، بیشتر بیمارانی که در لیست پیوند کبد قرار می گیرند امتیاز MELD بیشتر از ۲۵ دارند ( میلر ص ۲۲۸۶)
در پیوند کبد امتیاز MELD از جهت پیش آگهی بر چه نکته ای تاکید دارد؟
مورتالیتی ۹۰ روزه قبل پیوند کبد ( لیست انتظار) ( میلر ص ۲۲۸۶)
— امتیاز MELD به زبان خودمانی اینگونه می گوید که اگر پیوند کبد انجام نشود ، مورتالیتی ۹۰ روزه بیماران لیست انتظار چقدر است
— امتیاز MELD معیاری برای پیش بینی عوارض بعد از عمل پیوند کبد نیست !!
آیا امتیاز MELD محدودیت هایی نیز دارد ؟
— در مواردی همچون مسمومیت با استامینوفن این امتیاز قدرت پیشگویی کننده چندانی ندارد( میلر ص ۳۰۴۶)
— در کارسینوم هپاتوسلولار (HCC) نیز اتکاء به این امتیاز می تواند سبب شود تا بیمار امکان جراحی را از دست دهد ( میلر ص ۲۲۸۶) امتیاز بالای ۱۰ در اینگونه بیماران هشدار دهنده است( میلر ص ۲۲۵۹)
امتیاز CHILD چیست؟
این امتیاز نیز برای تخمین خطرات حول و حوش عمل در بیماران پیشرفته کبدی طراحی شده است و از اسم سه پزشک Child و Turcotte و Pugh گرفته شده است . تفاوت های امتیاز CHILD و MELD را در جدول ذیل ملاحظه می کنید :
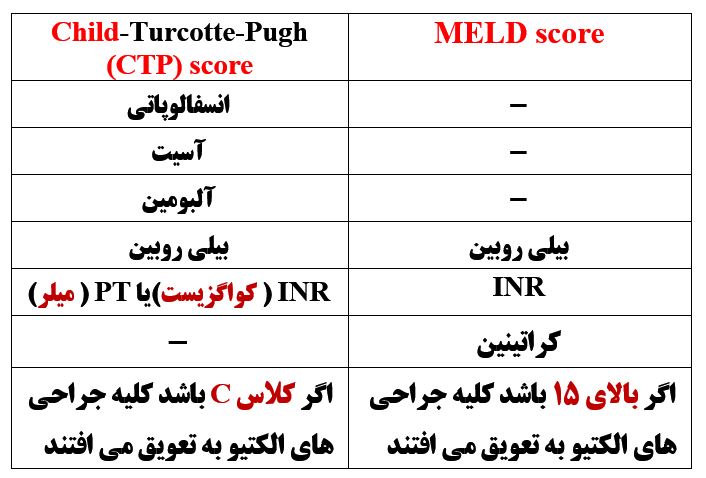
برای تخمین خطرات حول و حوش عمل در بیماران مبتلا به بیماری کبدی پیشرفته ، معیار CHILD بهتر است یا معیار MELD ؟ چرا ؟
گرچه هر دوی این امتیازات برای تخمین پیش آگهی در بیماران کبدی پیشرفته به کار می روند ( میلر ص ۱۹۳۲) ولی از سال ۲۰۰۲ سیستم CHILD جای خود را به MELD score داده است ( میلر ص ۲۲۸۵و ۱۱۲۲ و کواگزیست ص ۶۵) .دلایل برتری امتیاز MELD عبارتند از :
الف) عدم تاکید بر معاینات فیزیکی (همچون آسیت و انسفالوپاتی)
ب) معیاری پیوسته (continuous) است نه طبقه بندی شده ( categorical ). یعنی تخمین خطر در مورد یک دسته از بیماران نیست بلکه در مورد هر یک از بیماران است .
ج ) یکی از متغیرهای آن کراتینین است که اهمیت وضعیت کلیوی را در بیماری پیشرفته کبد یادآور می شود
=================================================================================================
در بیماران نارسائی کبد ( سیروز کبدی) که کاندید پیوند هستند ، رژیم تغذیه ای چگونه باید باشد؟( میلر ص ۳۱۵۳)
— پروتئین/ آمینواسید بالا ( به خاطر سرعت سنتز پروتئین بالا و نیز برای جایگزینی پروتئین از دست رفته به شکل آسیت )
— کالری بالا ( به دلیل هیپرمتابولیسم )
— محدودیت سدیم و مایعات / استفاده از دیورتیک ( برای کنترل آورلود مایع)
برای بیمارانی که در لیست انتظار پیوند کبد هستند و احتمال بیماری شریان کرونر( CAD ) در آنها بالا است ، کدامین روش ارزیابی قلبی را توصیه می کنید؟( میلر ص ۲۲۷۶)
آنژیوگرافی کرونر.
دلیل این امر آن است که خیلی از این بیماران نمی توانند تست ورزش را انجام دهند . استرس اکوکاردیوگرافی با دوبوتامین هم ارزش آماری تعیین کننده ای در این بیماران ندارد.
هیپوناترمی در بیماران کاندید پیوند کبد را در مرحله قبل از عمل چگونه باید درمان کرد؟
بیماران سیروزی بالقوه درمعرض خطر عارضه نورولوژیک central pontine myelinolysis قرار دارند . به همین خاطر نباید هیپوناترمی آنها را به شکل سریع تصحیح نمود . در گیرندگان پیوند کبد این تصحیح باید کمتر از 16 mEq/L باشد. ( میلر ص ۲۲۷۸ و ۲۲۸۲) ( خارج از کتب رفرنس / باراش : طی ۸ روز این هیپوناترمی را باید تصحیح نمود)
آیا نارسائی حاد کبدی (ALF) از اندیکاسیون های پیوند کبد است؟ ( میلر ص ۳۰۴۶)
بله . نارسائی حاد کبدی ( که در گذشته به آن نارسائی کبد فولمینانت گفته می شد) حدود ۴ درصد از موارد پیوند کبد را تشکیل می دهد. بدون پیوند کبد مورتالیتی ALF چیزی حدود ۶۰ تا ۸۰ درصد است. شایعترین دلیل ALF مسمومیت با استامینوفن است و در میان علل ALF همین مسمومیت با استامینوفن از مواردی است که امتیاز MELD در آن ارزش پیشگویی کننده خوبی ندارد . متاسفانه میزان موفقیت پیوند کبد در نارسائی حاد کبدی کمتر از نارسائی مزمن کبد است .علل مرگ در ALF عبارتند از ادم مغزی ، نارسائی متعدد ارگانها و سپسیس .
آیا در صورت وجود هیپرتانسیون پولمونر ، انجام پیوند کبد ممنوعیت مطلق دارد ؟( کواگزیست ص ۳۵۶)
در تعریف ، هیپرتانسیون پولمونر وجود فشار متوسط شریان ریوی بالاتر از ۲۵ میلی متر جیوه است .
تنها در صورتی که این فشار بالاتر از ۴۵ میلی متر جیوه شود ، پیوند کبد ممنوعیت مطلق دارد .
=================================================================================================
برای القاء بیهوشی در بیمار پیوند کبد ، در شکل معمول از کدام روش استفاده می شود؟( میلر ص ۲۲۸۱)
القاء سریع (rapid sequence) . انتخاب این روش به دلایل زیر است :
الف) ماهیت emergent جراحی
ب) استفاده از داروهای خوراکی (ایمونوساپرسانت های و آنتی بیوتیک ها) قبل عمل
ج) وجود آسیت
هوشبر استنشاقی انتخابی در پیوند کبد کدام هوشبر است؟ چرا ؟
ایزوفلوران . این انتخاب به دلیل آن است که ایزوفلوران جریان خون اسپلانکنیک را بهتر از هوشبرهای استنشاقی دیگر حفظ می کند.
شل کننده عضلانی انتخابی حین عمل پیوند کبد کدام دارو است ؟
سیس آتراکوریوم( Cisatracurium) . این انتخاب به دلیل آن است که دفع این دارو مستقل از ارگان است و هیستامین آزاد نمی کند.
قبلا در مورد آتراکوریوم تصور می شد که laudanosine حاصل از آن تجمع کرده و سبب مشکلات کبدی می شود ولی بعدا مشخص شد که این موضوع اهمیت بالینی ندارد ( میلر ص ۹۸۸)
بیمار مبتلا به نارسائی کبد فولمینانت (ALF) که ادم مغزی نیز دارد تحت پیوند کبد قرار دارد . در این بیمار چگونه از هوشبراستنشاقی استفاده می شود؟
در این بیمار یا از هوشبراستنشاقی اجتناب می کنیم و یا از مقادیر کم آن به همراه مانیتورینگ ICP استفاده می کنیم.
در بیمار پیوند کبدی که حین جراحی دچار افت فشارخون می شود چگونه از هوشبراستنشاقی استفاده می کنیم؟
هوشبر استنشاقی را موقتا قطع کرده و طی این زمانها از میدازولام استفاده می کنیم.
آیا استفاده از کاتتر شریان ریوی برای مانیتورینگ حین پیوند کبد اجباری است؟
استفاده از کاتتر شریان ریوی در مانیتورینگ پیوند کبد کمک کننده است ولی اگر ارزیابی های اخیر بیمار، شواهدی از افزایش فشارخون شریان ریوی ندارد ، نیازی به استفاده از این کاتتر نیست .
آیا می توان از نایتروس اکسید (N2O) در بیهوشی پیوند کبد استفاده کرد؟
– در چاپ های قبلی میلر نوشته شده بود که به دلیل اتساع روده ها و بدتر شدن دید جراح نباید از N2O در پیوند کبد استفاده شود
– در چاپ فعلی میلر در این باره اظهار نظری نشده است (و این تاکید تنها در مورد پیوند کلیه قید شده است) .
– خارج از امتحان: در کتب دیگری همچون باراش ۲۰۱۷ همچنان تاکید شده که نباید از N2O در بیهوشی پیوند کبد استفاده شود
نکات بیهوشی پیوند کبد:
— کاتتر شریانی عمدتا بلافاصله بعد از القاء بیهوشی قرار داده می شوند ولی قبل از القاء هم می شود
— از یک یا دو رگ بزرگ ( در مواردی که احتمال خونریزی بالا وجود دارد) به شکل مرکزی استفاده می شود
— استفاده از TEE حین عمل فراوان است( احتمال کم عوارض خونریزی دهنده حتی در حضور واریس مری)
— سیستم تزریق سریع ( برای ترانسفوزیون خون بالاتر از نیم لیتر در دقیقه)
پاره ای از داروها دارای متابولیسم خارج کبدی هستند و قاعدتا در بیماریهای کبدی و نیز فاز anhepatic کبدی تغییر چندانی ندارند . این داروها کدامند؟
مورفین ، پانکرونیوم ، سوکسنیل کولین ، پروپوفول ، رمی فنتانیل ، اسمولول از جمله داروهایی هستند که متابولیسم خارج کبدی دارند ولی در دو مورد رمی فنتانیل و پروپوفول ( میلر صفحات ۸۲۳ و ۸۹۲) قید شده که فارماکوکینتیک آنها طی فاز anhepatic پیوند کبد تغییر نمی کند .
برای کنترل درد بعد از عمل بیماران پیوند کبد از چه روش هایی استفاده می کنید؟
در پیوند کبد (در مقایسه با دیگر اعمال شکمی ماژور) نیاز به داروی آنالژزیک کمتری است و کنترل درد بعد عمل عمدتا با بیدردی کنترل شده توسط بیمار(PCA) است .
بعد از درآوردن لوله تراشه ، به غیر از PCA از دوزهای بینابینی بولوس مخدرهای وریدی ( همچون فنتانیل یا هیدرومورفون) نیز می توان استفاده کرد. (کواگزیست ص ۳۵۷)
چرا برای کنترل درد بعد از عمل پیوند کبد نمی توان از آنالژزی اپیدورال استفاده کرد؟
آنالژزی اپیدورال به دلیل کواگولوپاتی ممنوع است . این کواگولوپاتی یا از قبل وجود داشته و یا طی جراحی ایجاد می شود ( حتی در صورت نرمال بودن تست های انعقادی و یا بعد از اصلاح اختلال انعقادی نیز نمی توان از آنالژزی اپیدورال برای کنترل درد بعد عمل استفاده کرد)
انجام بلوک عصب اینترکوستال برای کنترل درد بعد از عمل پیوند کبد کمک کننده است ( میلر ص ۲۴۴۶)
بعد از انجام پیوند کبد ، چه زمانی لوله تراشه بیمار را خارج می کنیم ؟
زمان دقیق درآوردن لوله تراشه و قطع ونتیلاتور بعد از پیوند کبد دقیقا مشخص نیست و نظرات متفاوت است 🙁 میلر ص ۲۲۸۴ و کواگزیست ص ۳۵۷)
میلر ص ۲۲۸۴ : در خیلی از مراکز پیوند کبد ، قبل از درآوردن لوله تراشه از علائم clear عملکرد گرافت مطمئن می شوند.
کواگزیست ص ۳۵۷ : بهتر است بیماران در ICU چند ساعت زیر ونتیلاتور قرار گیرند تا اسیدوز متابولیک آنها برطرف شود و عملکرد گرافت بهبود یابد و سونوگرافی RUQ برای اطمینان از باز بودن عروق انجام شود.
میلر ص
=================================================================================================
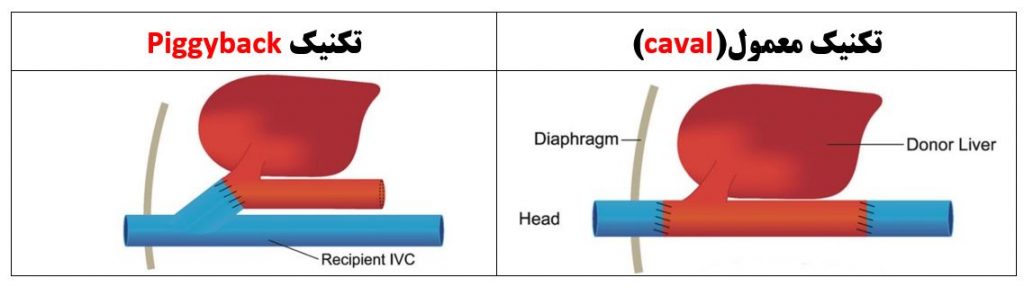
حداقل از دو تکنیک جراحی برای پیوند کبد استفاده می شود . این تکنیک ها کدامند؟
الف) تکنیک معمول که به تکنیک caval مشهور است و طی آن کراس کلامپ کامل عروق ( IVC و ورید پورتال و شریان کبدی) انجام می شود. با انجام این تکنیک حدود ۵۰ درصد از بازگشت وریدی و برون ده قلبی افت می کند و گاهی برای مقابله با آن از بای پس وریدی – وریدی (VVB) استفاده می شود
ب) تکنیک Piggyback : در این تکنیک قسمت رتروهپاتیک IVC فرد گیرنده باقی می ماند و به همین دلیل افت بازگشت وریدی شدید نیست و و کاهش آن با وازوپرسور ، کریستالوئید و کلوئید جبران می شود. طبیعتا در این روش که به شکل پارشیال کراس کلامپ است دیگر نیازی به بای پس وریدی – وریدی (VVB) نیست . ( ص ۱۸۰۸ و ۲۲۸۱ و ۲۲۸۲ و ۲۲۸۳)
تصویر زیر ( خارج از رفرنس ) به شکلی ساده تفاوت این دو تکنیک را نشان می دهد. قسمتهای آبی رنگ مربوط به گیرنده پیوند و قسمت های قرمز مربوط به دهنده پیوند است :
آیا استفاده از بای پس وریدی – وریدی (VVB) در پیوند کبد اجباری است؟( میلر ص ۲۲۸۳)
خیر . آنچنان که در سوال قبل گفته شد استفاده از تکنیک مرسوم Caval به دلیل کراس کلامپ کامل عروق ، سبب کاهش شدید بازگشت وریدی می شود و برای مقابله با آن از VVB استفاده می شود . این بای پس سبب می شود که خون از IVC (از مسیر ورید پورتال و سپس ورید آگزیلاری ) به SVC دایورت شود .
—- مزایای VVB: برطرف کردن مشکل پره لود ، بهبود فشار پرفوزیون کلیوی ، کاهش احتقان اسپلانکنیک ، تاخیر ایجاد اسیدوز متابولیک
—- خطرات VVB : آمبولی هوا ، ترومبوآمبولیسم
مصرف VVB اجباری نیست و در تکنیک Piggyback ( که پارشیال کراس کلامپ است) آنچنان کاربردی ندارد
=================================================================================================
پس از انجام هپاتکتومی دهنده ، برای خنک نگاه داشتن و جابجايی کبد عمدتا از دو محلول استفاده می شود . این دو محلول کدامند؟( میلر ص ۲۲۹۷)
— محلول دانشگاه ویسکانسین ( UW ): شایعترین محلول است و پتاسیم آن به شکل قابل ملاحظه ای از محلول HTK بالاتر است
— محلول هیستیدین – تریپتوفان- کتوگلوتارات ( HTK ): عملکرد گرافت ضعیف تر است
با توجه به اینکه پتاسیم محلول UW بسیار بیشتر از پتاسیم محلول HTK می باشد آیا می توان نتیجه گرفت که طی ری پرفیوژن کبد ، محلول UW بیشتر سبب هیپر کالمی شدید می شود ؟
فارغ از اینکه از کدام محلول برای نگهداری گرافت استفاده شود ، امروزه به منظور کاهش خطر هیپرکالمی شدید ( و قبل از ری پرفیوژن) گرافت را با کلوئید شستشو می دهند ( میلر ص ۲۲۹۷) بنابر این قضاوت بالا در عمل صحیح نیست.
cold ischemia time برای کبد پیوندی چقدر است ؟( میلر ص ۲۲۹۷)
ریه ( ۴ ساعت)/ قلب ( ۶ ساعت)/ کبد ( ۱۲ ساعت) / کلیه ( ۲۴ ساعت)
=================================================================================================
پیوند کبد به سه فاز تقسیم می شود . این سه فاز کدامند ؟ ملاحظات بیهوشی در هر کدام از این فازها چیست ؟( جدول کواگزیست ص ۳۵۷)
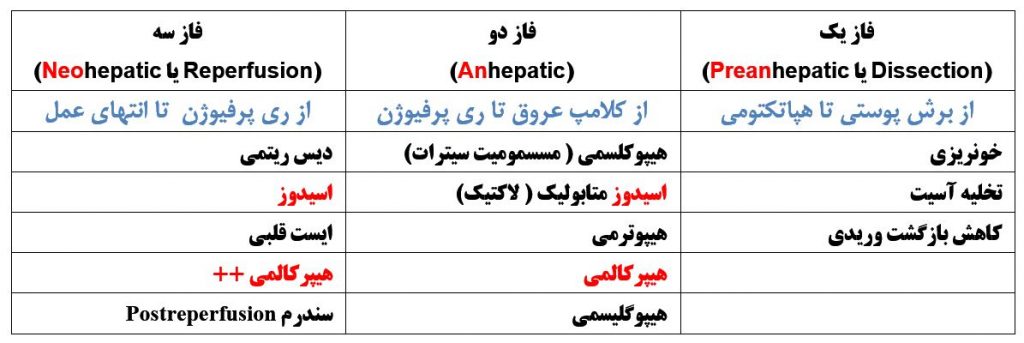
دو عامل اصلی کاهش حجم طی فاز preanhepatic کدامند؟
— خونریزی قابل توجه
— تخلیه آسیت
خونریزی در خلال فاز preanhepatic تحت تاثیر چه عواملی است ؟( میلر ص ۲۲۸۳)
— درجه کواگولوپاتی از قبل موجود
— حضور و شدت پورتال هیپرتانسیون
— مدت زمان و پیچیدگی جراحی (که با جراحی های قبلی شکمی و چسبندگی های آن بدتر می شود )
چرا باید طی پیوند کبد از هیپرگلیسمی پرهیز نمود ؟ ( میلر ص ۲۲۸۳)
چون گلوکز بالای ۱۸۰ میلی گرم / دسی لیتر سبب عفونت محل جراحی می شود
هیپوکلسمی یونیزه یکی از مشکلات بیهوشی پیوند کبد است. هیپوکلسمی در کدام فاز پیوند کبد شایعتر است و ناشی از چیست؟( میلر ص ۱۸۵۰ و ۲۷۸۵ و کواگزیست ص ۳۵۷)
هیپوکلسمی یونیزه بیشتر در فاز anhepatic و به دلیل ترانسفوزیون روی می دهد. یعنی سیترات ناشی از فرآورده خونی وارد بدن می شود. در حالت معمول کبد اقدام به متابولیزه سیترات ناشی از ترانسفوزیون می کند ولی در اینجا که کبدی وجود ندارد (anhepatic) ناچارا سیترات متصل به کلسیم یونیزه شده و در نهایت هیوکلسمی یونیزه ایجاد می کند.
— یکی از مهمترین مواردی که در آن مسمومیت سیترات دیده می شود همین جراحی پیوند کبد است.
— علائم مسمومیت سیترات : افت فشار خون ، فشار نبض باریک ، افزایش CVP ، افزایش فشار پایان دیاستولی داخل بطن .
— عمدتا سیترات موجود در FFP بیش از سیترات موجود در خون کامل است و به همین جهت تجویز FFP با سرعت بالا شایعترین دلیل هیپوکلسمی یونیزه است.
— استفاده از کلسیم اگزوژن ( کلرید کلسیم یا گلوکونات کلسیم) در اینگونه موارد ضرورت دارد.
—البته وقوع مسمومیت سیترات در فاز Preanhepatic هم امکانپذیر است ولی چون در این فاز هنوز کبد وجود دارد احتمال آن کمتر است ( میلر ص ۲۲۸۲)
آریتمی و ترومبوآمبولی (داخل قلبی) ممکن است در هر کدام از فازهای پیوند کبد روی دهد ولی در کدام فاز شایعتر است ؟
بعد از ری پرفیوژن شایعتر است ( میلر ص ۲۲۸۳)
هیپرکالمی در کدام فاز پیوند کبد رخ می دهد؟ برای مقابله با آن چکار باید کرد؟
گرچه هیپرکالمی در فاز anhepatic هم روی می دهد ( کواگزیست ص ۳۵۷) ولی هیپرکالمی شدید و کشنده عمدتا در فاز reperfusion دیده می شود .
در فاز preanhepatic گرچه خطر هیپرکالمی وجود ندارد (ولی به منظور اینکه از خطر هیپرکالمی در فاز reperfusion کاسته شود) نباید در این فاز اقدام به درمان تهاجمی هیپوکالمی نمود .
در فاز anhepatic نیز (برای اینکه از خطر هیپرکالمی در فاز reperfusion کاسته شود) باید اقدام به نرمال کردن PH و نگهداری پتاسیم در محدوده low normal کرد . این کار را می توان با کلسیم ، انسولین- دکستروز ، هیپرونتیلاسیون و حتی بیکربنات سدیم نمود.
اما هیپرکالمی کشنده عمدتا در فاز reperfusion روی می دهد . از جهت بالینی این هیپرکالمی حاد خود را با تغییرات در EKG نشان می دهد و نیاز درمان فوری دارد .درمان انتخابی آن در اینگونه موارد استفاده از کلرید کلسیم و بیکربنات سدیم هستند. اگر زمان کافی داشته باشیم می توان از آلبوترول و انسولین نیز استفاده کرد .
postreperfusion syndrome در پیوند کبد چیست ؟( میلر ص ۲۲۸۳ , ۱۸۰۸)
سندرم postreperfusion در یک سوم موارد در اوایل فاز نئوهپاتیک روی می دهد و عمدتا ناشی از برداشتن کلامپ از ورید پورتال و آزاد شدن مایعات سرد ، پتاسیم و اسید به داخل سیرکولاسیون است .
هالمارک آن افت فشارخون سیستمیک (کاهش SVR) + هیپرتانسیون ریوی است که طی اولین ۵ دقیقه بعد ریپرفیوژن گرافت اتفاق می افتد. در این حالت افزایش حاد CVP ( پره لود) نیز روی می دهد
علت اصلی شناخته نیست ولی پاره ای عوامل مطرح شده عبارتند از : هیپرکالمی ، اسیدوز ، هیپوترمی ، آمبولی ( هوا یا ترومبوتیک)، مواد وازواکتیو
ریسک فاکتورهای هیپرکالمی در این دوره عبارتند از :
— افزایش سطح پتاسیم در مرحله preanhepatic
— اهداء عضو بعد از مرگ قلبی
مشکل فیبرینولیز بیشتر در کدام مرحله پیوند کبد خود را نشان می دهد؟
— فیبرینولیز در خلال فاز preanhepatic غیرمعمول است . و معمولا شروع فیبرینولیز از فاز anhepatic است .
— شدیدترین فیبرینولیز را معمولا متعاقب reperfusion داریم . علت این امر افزایش در فعال کننده پلاسمینوژن بافتی (tPA) است که از سلول های اندوتلیال گرافت آزاد می شود. برای درمان ممکن است نیاز به کرایو و آنتی فیبرینولیتیک داشته باشیم.( میلر ص ۲۲۸۴)
آیا می توان از recombinant activated factor VII به منظور کاهش ترانسفوزیون حین پیوند کبد استفاده کرد؟
خیر ولی rfVIIa می تواند سبب بهبود پاره ای مشکلات انعقادی حین عمل شود . از عوارض جانبی آن افزایش ترومبولی شریانی ( نه وریدی ) می باشد ( میلر ص ۱۸۴۸ و
ترومبوز شریان کبدی چگونه خود را نشان می دهد؟
طی ۲ تا ۳ روز اول بعد پیوند کبد ، سطح ترانس آمیناز ها ممکن است (به علت ایسکمی گرافت یا صدمه طی جراحی پیوند) غیرطبیعی باشد و این نکته ایرادی ندارد . ولی اگر بعد از این مدت آنزیم های کبدی و بیلی روبین کاهش نیابند احتمال ترومبوز شریان کبدی بالا می رود. این مورد یکی از عوارض شدید بعد از پیوند کبد است که ممکن است منجر به نکروز گرافت و در نهایت پیوند مجدد شود ( میلر ص ۲۲۸۴) . جهت تشخیص فورا باید اولتراسونوگرافی داپلر انجام شود. این عارضه در اطفال به دلیل قطر تنگ تر رگ ها شایعتر است . ( میلر ص ۲۲۸۸)
بعد از عمل پیوند کبد ، چگونه اقدام به ارزیابی عملکرد گرافت کبدی می شود ؟
—- مواردی که در اتاق عمل و بلافاصله بعد عمل کنترل می شود : ( میلر ص ۲۲۸۳ و ۲۲۸۴) کاهش نیاز به کلسیم ، بهبود اسیدوز ، افزایش مقدار ادرار ، افزایش دمای مرکزی، خروج صفرا
—- مواردی که طی ساعاتی پس از تکمیل جراحی مشاهده می شود : بهبود وضعیت نورولوژیک ، ثبات قلبی عروقی ، بهبود عملکرد کلیه
برای ارزیابی عملکرد گرافت از سطح ترانس آمینازها ، PT ، سطح بیلی روبین ، خروجی صفرا و ادرار و وضعیت اسید – باز کمک گرفته می شود
یکی از عوارض بعد از پیوند کبد عبارت است از primary nonfunction of the graft است . علائم این عارضه کدامند؟ چکار باید کرد؟( میلر ص ۲۲۸۴ )
این عارضه عمدتا شامل عدم وجود صفرا و بی ثباتی همودینامیک است و بیمار ممکن است نیاز به پیوند urgent داشته باشد .
=================================================================================================
از داروهای سرکوبگر سیستم ایمنی (ایمونوساپرسانت ها) به منظور جلوگیری از پس زدن پیوند استفاده می شود . عوارض این داروها کدامند؟
— افزایش شانس عفونت
— اثرات جانبی بر روی ارگانهای بدن
— افزایش شانس بدخیمی در گیرنده پیوند
البته باید دانست که گیرنده های پیوند کبد ( نسبت به سایر پیوندها) نیاز به ایمونوساپرسانت کمتری دارند .
کدامیک از ایمونوساپرسانت ها از طریق مهار آنزیم کلسی نورین (Calcineurin) عمل می کنند؟
سیکلواسپورین و تاکرولیموس . کلسی نورین آنزیم مهمی جهت فعال سازی T-cell ها است . یعنی در واقع محل اثر این داروها در سلول های T-helper هست . ( میلر ص ۲۲۸۸ و کواگزیست ص ۳۷۰ و ۶۰۷). دقت کنید سیرولیموس از این طریق عمل نمی کند.
اثرات جانبی داروهای مهارگر کلسی نورین کدامند؟
الف) توکسیسیتی کلیوی : این داروها در اثر تنگی عروق آوران و کاهش GFR سبب مشکلات کلیوی می شوند که در نهایت منجر به افزایش کراتینین می شود . این ازتمی معمولا در مراحل اولیه با کاهش دوز قابل برگشت است . برای مقابله با این مشکل بیمار قبل از عمل باید هیدراسیون کافی داشته باشد و در حین عمل هم از دادن هوشبرهایی که کلیرنس کلیوی دارند خودداری کنیم ( کواگزیست ص ۱۰۴) بعد از عمل نیز حتما باید کلیرنس کراتینین ارزیابی شوند .
ب) توکسیسیتی نورولوژیک : ترمور ، سردرد ، تشنج و حتی مشکلات نورولوژیک فوکال
ج) هیپرتانسیون: به شکل تیپیک طی هفته اول درمان به دلیل تنگی عروق و احتباس سدیم ایجاد می شود.
آیا نفروتوکسیسیتی تاکرولیموس کمتر از سیکلواسپورین است ؟
خیر . نفروتوکسیسیتی این دو دارو تفاوتی با هم ندارد ( میلر ص ۵۸۰)
استفاده همزمان داروهای بلوکر کانال کلسیم با داروهایی همچون سیکلواسپورین یا تاکرولیموس سبب چه تغییری می شود؟
سبب افزایش سطح پلاسمایی این داروها می شود . به همین خاطر معمولا دوز این داروها را کاهش می دهند و در نتیجه نفروتوکسیسیتی آنها کاهش می یابد.
آیا سیکلواسپورین تاثیری بر شل کننده های عضلانی دارد؟
سیکلواسپورین سبب تسهیل بلوک و تاخیر متابولیسم پاره ای شل کننده های عضلانی مثل پانکرونیوم و وکورونیوم می شود ولی نیازی به تغییر دوز این شل کننده ها نیست ( کواگزیست ص ۱۰۵ و ۵۵۷)
رایجترین داروی ایمونوساپرسانت در پیوند کبد کدام است؟
تاکرولیموس ( با نام تجاری پروگراف)
آیا سیرولیموس (Sirolimus) نیز همانند تاکرولیموس از مهارگران کلسی نورین است ؟
خیر .سیرولیموس دارویی ایمونوساپرسانت است که مکانیسم اثر آن از طریق مهارپروتئین mTOR است . ( میلر ص ۲۲۸۸) صدمه کلیوی سیرولیموس بسیار کمتر از دو داروی قبلی است و همچنین کاربرد توام این دارو با سیکلواسپورین یا تاکرولیموس سبب کاهش دوز و در نتیجه کاهش توکسیسیتی کلیوی طولانی مدت آنها می شود ( میلر ص ۵۸۱ و ۲۸۳۹ )
از آثار جانبی سیرولیموس می توان به میلوساپرسیون ( آنمی ، ترومبوسیتوپنی و لکوپنی) اشاره کرد ( میلر ص ۱۱۳۷)
استفاده از سیرولیموس (بر عکس داروهای قبلی) سبب افزایش خطر سرطان نمی شود بلکه برای این دارو اثرات ضد توموری نیز ذکر شده است ( میلر ص ۲۲۸۹)
خلاصه ای از سه داروی ایمونوساپرسانت در پیوند کبد:

=================================================================================================
بیماری که قبلا تحت عمل پیوند کبد قرار گرفته است برای عمل جراحی ( غیرمرتبط به پیوند) مراجعه کرده است . ملاحظات بیهوشی در این بیمار کدامند؟( میلر ص و کواگزیست ص ۵۵۶ و ۵۵۷)
— بهترین مارکر برای ارزیابی عملکرد سنتتیک کبد PT یا INR است .
— رعایت استریلیتی اهمیت فوق العاده ای دارد
— در بیمارانی که به شکل مزمن از کورتیکواستروئید استفاده می کنند تجویز استرس دوز کورتیکواستروئید اهمیت دارد
— به دلیل استفاده از ایمونوساپرسانت ها ، باید عملکرد کلیوی را ارزیابی کرد
— باید از داروهایی که کاهش جریان خون کبدی ( مثل پروپرانولول) دارند اجتناب نمود
— اگر وضعیت انعقادی مشکلی ندارد می توان از بی حسی رژیونال استفاده کرد ولی باید توجه داشت که بیهوشی عمومی اثر ایمونوساپرسانت بیشتری نسبت به بی حسی رژیونال دارد
— باید از لوله گذاری از طریق بینی خودداری کرد چون ممکن است سبب ورود فلور باکتریال بینی به داخل سیرکولاسیون سیستمیک شود
— بیماری که عفونت فعال دارد باید تا مشاوره جراحی یا به تاخیر افتد و یا کنسل شود
— تمام داروها و آنتی بیوتیک هایی که بیمار دریافت می کند بررسی و سرتاسر عمل ادامه یابند.
بیماری که قبلا پیوند کبد شده و در حال حاضر شواهدی از پس زدن فعال(active rejection) دارد جهت جراحی مراجعه کرده است . چه اقدامی باید کرد؟
در حالت معمول انجام هرگونه عمل الکتیوی ممنوع است ولی اگر جراح قصد explantation ارگان پیوند شده را دارد انجام عمل اورژانس تلقی می شود ( کواگزیست ص ۵۵۷)
=================================================================================================
اکثریت اهداء کبدها از طرف بیماران مرگ مغزی صورت می گیرد. آیا اهداء کبد از سوی دهنده زنده نیز انجام می شود؟ ( میلر ص ۲۳۰۳ تا ۲۳۰۵)
بله . اکثر پیوندهای کبد ازسوی دهندگان زنده (LDLT) در مورد نارسائی های مزمن کبدی و در شرایط الکتیو انجام می شود ( ولی موارد غیرشایعی همچون نارسائی حاد کبدی (ALF) وجود دارد که پیوند کبد به شکل اورژانسی انجام شده است).
— اکثریت هپاتکتومی ها در اینگونه موارد هپاتکتومی چپ است ( مزیت هپاتکتومی چپ نسبت به هپاتکتومی راست : پیچیدگی کمتر ، زمان کوتاهتر ، انجام راحت تر و خطرات و عوارض کمتر ).
— دو تا سه هفته بعد از برداشتن دوسوم کبد ، سایز کبد به میزان اولیه باز می گردد.
— گیرنده های پیوند می توانند اطفال و یا بزرگسال باشند.
ملاحظات بیهوشی در اهداء کبد از سوی دهنده زنده (LDLT) کدام است؟
— ابتدا توسط متخصص بیهوشی (با دهنده کبد و خانواده وی) توضیحاتی درباره خطرات و نگرانی های عمل داده می شود
— در شروع عمل پوزیشن بیمار به حالت سوپاین و در حین عمل به حالت ریورس ترندلنبرگ است ( برای تسهیل دستیابی جراح به کبد)
— از بیهوشی عمومی با شل کننده عضلانی استفاده می شود
— دو رگ بزرگ لازم است
— معمولا از مانیتور غیرتهاجمی استفاده می شود
— از NG tube استفاده می شود ( برای دکپرس معده و دید بهتر جراح)
— در برخی مراکز در خلال هپاتکتومی حفظ CVP در مقادیر پائین ( کمتر از ۵ سانتی متر آب) برای کاهش خونریزی و ترانسفوزیون انجام می شود.
— در اکثریت مراکز لوله تراشه بیمار در انتهای عمل در آورده شده و بیمار به ریکاوری منتقل می شود .اغلب نیازی به انتقال بیمار به ICU نیست .
بیماری به عنوان دهنده زنده پیوند کبد (LDLT) تحت بیهوشی قرار می گیرد . طی آزاد سازی کبد و عروق آن بیمار دچار دفعاتی از افت فشارخون می شود. آیا علت این امر خونریزی است ؟
خیر . اکثریت خونریزی در خلال ترانسکشن پارانشیم کبد اتفاق می افتد . افت فشار خون در این مورد بیشتر به دلیل کاهش بازگشت وریدی ناشی از دستکاری کبد است و معمولا مشکل با برگشت کبد به موقعیت اصلی آن برطرف می شود. اگر افت فشارخون برطرف نشد بناچار از داروهای کوتاه اثر وازواکتیو یا مایع استفاده می کنیم .
در مورد کنترل درد بعد از عمل در اهداء کنندگان زنده کبد چگونه عمل می کنید؟
— در مورد بی حسی اپیدورال اختلاف نظر وجود دارد ولی نگرانی از کاتتر اپیدورال به خاطر احتمال کواگولوپاتی بی مورد است . در هر صورت اگر کاتتر اپیدورال گذاشته شود ، این کاتتر نباید تا ۳ تا ۵ روز بعد که پارامترهای انعقادی طبیعی شوند برداشته شود .
— اگراز کاتتراپیدورال استفاده نشود می توان از PCA استفاده کرد
— در مورد مصرف آنالژزیک و مخدر در دوره بلافاصله بعد عمل باید احتیاط کرد
شایعترین عارضه بعد عمل در میان دهندگان زنده کبد کدام است ؟
عفونت .
عوارض بعد عمل در دهندگان زنده کبد با کدام موارد مرتبط هستند؟
— کراتینین قبل عمل بالاتر
— افت فشارخون حین عمل
— ترانسفوزیون حین عمل
=================================================================================================
خارج از امتحان :
باراش : به دلیل تاثیر منفی هیپوناترمی بر روی وضعیت کبدی بیماران ، از ژانویه ۲۰۱۶ مقدار سدیم هم به امتیاز MELD اضافه شده است . به نحوی که به این معیار MELD-Na گفته می شود.
باراش : انجام دیالیز طی دو هفته اخیر نیز تاثیر منفی بر روی امتیاز MELD دارد.
— برای محاسبه امتیاز MELD نرم افزارهای متعددی طراحی شده که شما می توانید بر روی تلفن همراه خود داشته باشید . با کلیک بر روی عکس زیر می توانید یکی از این نرم افزازها را از Google play دانلود و بر روی تلفن همراه خود نصب نمائید :
باراش : در اطفال زیر ۱۲ سال به جای امتیاز MELD ، از امتیاز PELD استفاده می شود که شامل ۵ متغیر است : بیلی روبین ، INR ، آلبومین ، سن و تاخیر رشد
باراش : برای کنترل درد بعد عمل بیماران پیوند کبدی می توان از TAP block استفاده کرد
باراش : برای تصحیح هیپوکلسمی یونیزه حین پیوند کبد ، استفاده از حالت انفوزیون نسبت به حالت بولوس برتری دارد چون شکل بولوس سبب استفاده بیش از حد کلسیم و نوسانات نسبتا زیاد کلسیم می شود
==================================================================================================================
— اولین پیوند کبد ایران ( در شیراز) توسط استاد دکتر سید علی ملک حسینی در اردیبهشت ۱۳۷۲ انجام شد. تا انتهای سال ۱۳۹۷ حدود ۶۵۰۰ پیوند کبد در ایران انجام شده که ۹۲ درصد این پیوندها از بیماران مرگ مغزی و مابقی پیوندها مربوط به اهداکنندگان زنده (فقط بستگان فرد گیرنده) بوده است.
==================================================================================================================
توجه داشته باشید این آزمون صرفا برای کمک به یادگیری یک “مفهوم بیهوشی” ارائه شده و هیچگونه امتیاز یا اطلاعاتی در این سایت ذخیره نمی شود.
falseit is false
falseit is false
falseit is false
falseit is false
falseit is false



